
令人满意的感染治疗高度依赖于早期诊断并及时干预。在难治性感染和感染复发中,抑制抗生素耐受型细菌可能是阻断细菌向耐药演变和根除病原体的治疗关键点。迄今为止,尚无针对抗生素耐受型细菌的治疗药物被批准。
2022年11月4日,国际顶刊Nano Today(IF 18.962)在线发表了上海交通大学医学院附属第九人民医院汤亭亭教授和杨盛兵副研究员团队的创新研究成果“Multi-roles of nanoscale bismuth metal-organic frameworks: Infectious photoacoustic probe and inhibitor of antibiotics tolerant bacteria via targeting endogenous H2S”。该研究利用光声成像技术成功检测了早期细菌感染,并利用Bi-MOF作为感染探针、抗生素载体和增强剂根除了抗生素耐受型细菌的感染。这一创造性策略为抗生素耐受型细菌的相关感染治疗提供了启示。其中,中科新生命提供了TMT蛋白质组+代谢组检测服务。

研究材料
野生型和甲氧西林耐受型MRSA
步骤1:野生型和抗生素(甲氧西林)耐受型(金黄色葡萄球)菌中的H2S水平;
步骤2:Bi-MOF表征及其作为细菌感染光声成像(PAI)探针的研究;
步骤3:Bi-MOF增强了甲氧西林对耐受型菌株的杀菌效果,并通过降低胞内H2S水平防止其产生;
步骤5:Bi-MOF在体内感染早期检测中的应用;
步骤6:Bi-MOF在耐受型菌株诱导的小鼠皮下感染模型中可协同增强甲氧西林的治疗效果并抑制感染复发。
研究结果
1. 野生型和抗生素(甲氧西林)耐受型(金黄色葡萄球)菌中的H2S水平
通过循环抗生素暴露演化法,研究人员基于野生型MRSA获得了耐甲氧西林MRSA (ATCC 25923) ,以下简称(抗生素)耐受型菌株。用H2S荧光探针和pb(ac)2检测法测定野生型和耐受型菌株的细胞内H2S水平。结果表明,耐受型菌株的H2S水平高于野生型 (图1D-F)。胞内H2S定量分析显示,耐受型菌株的胞内H2S水平显著高于野生型(图1E)。这些结果表明,在耐受型菌株中,H2S发生上调。
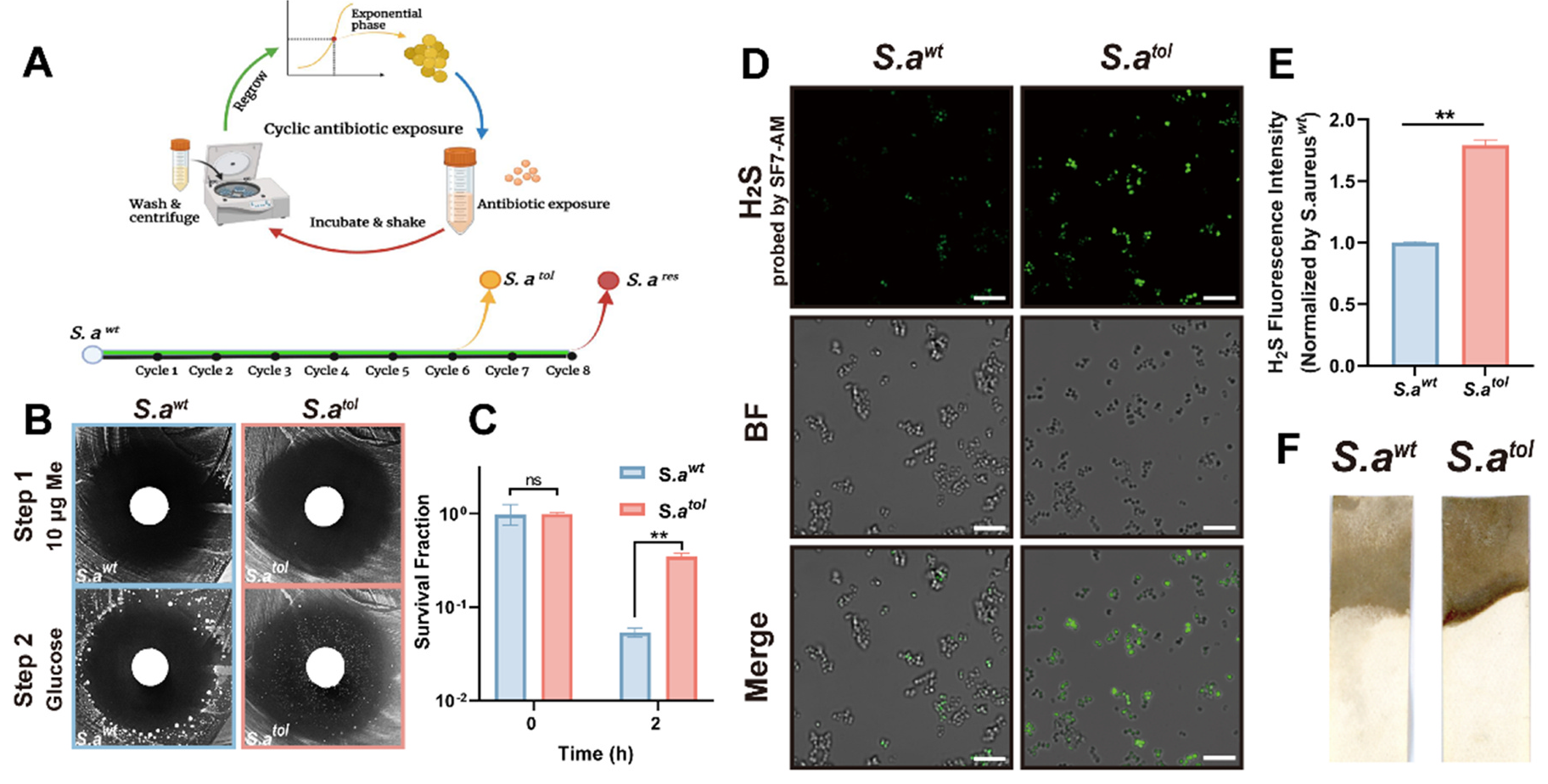
图1 耐甲氧西林MRSA对甲氧西林耐受性演变和胞内H2S水平提高
2. Bi-MOF表征及其作为细菌感染PAI探针的研究
未经处理的MRSA接种物经过Bi-MOF处理12 h后,颜色由浅黄色变为黑色(图2D),通过PAI信号测试,证实Bi-MOF可以作为细菌感染检测探针(图2E-F)。结合XRD谱图和透射电镜观察的结果发现,Bi-MOF与胞内H2S反应形成Bi2S3,其在激光照射下可发出PAI信号(图2H-G)。因此,Bi-MOF可作为细菌感染的PA检测探针。
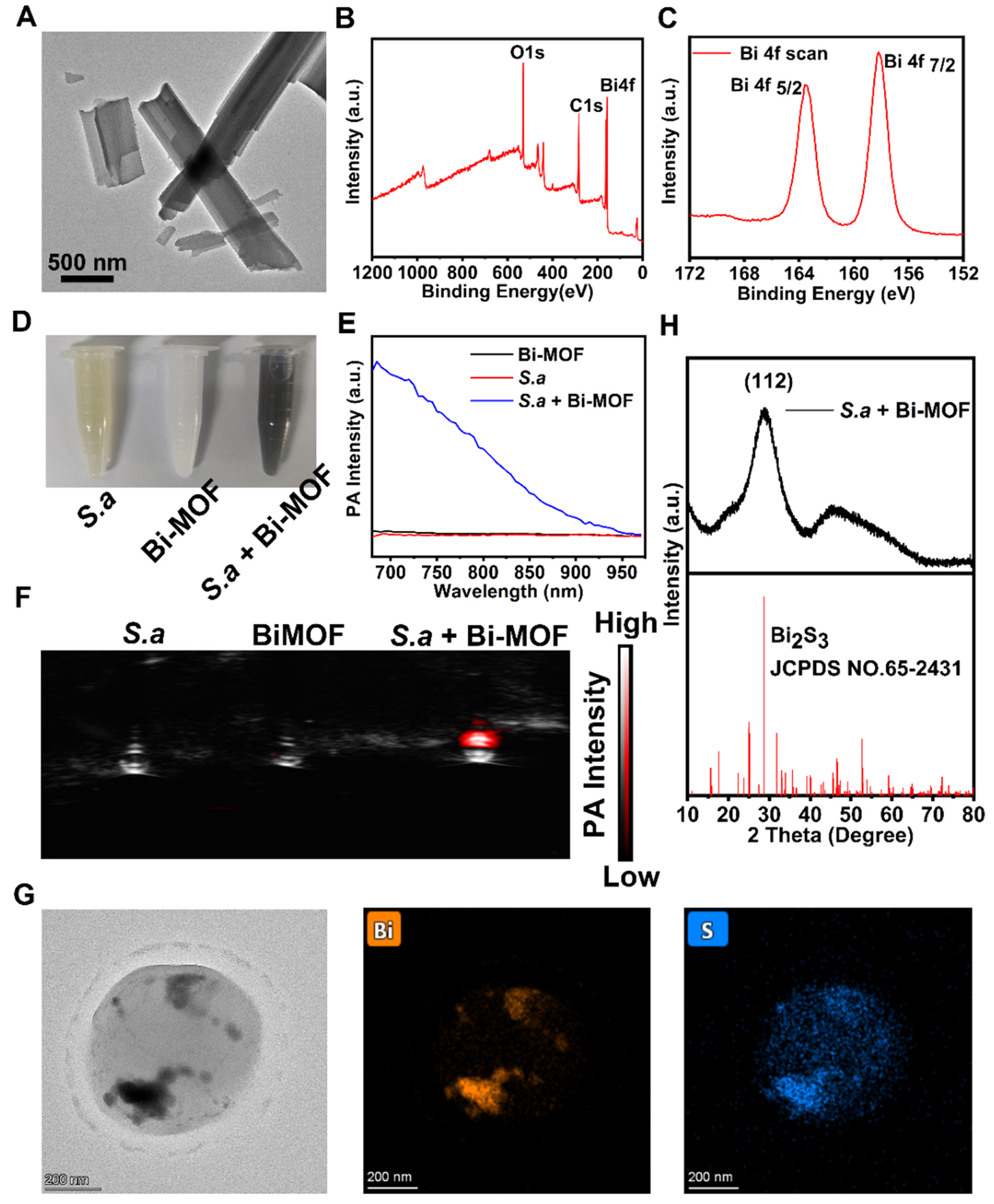
图2 Bi-MOF相关表征及其作为体外细菌感染光声(PA)诊断探针的性能
3. Bi-MOF增强了甲氧西林对耐受型菌株的杀菌效果,并通过降低胞内H2S水平防止其产生
通过两种独立的方法研究了在正常和抗生素应激条件下,Bi-MOF对耐受菌H2S的影响。结果证实,无论是在正常状态下还是在抗生素压力下,Bi-MOF治疗都有效地下调了耐甲氧西林MRSA的细胞内H2S水平。随后,又通过其他检测发现Bi-MOF能使耐受菌对甲氧西林敏感(图3E-G),并协同增强甲氧西林对耐受菌株的杀菌作用(图3I)。
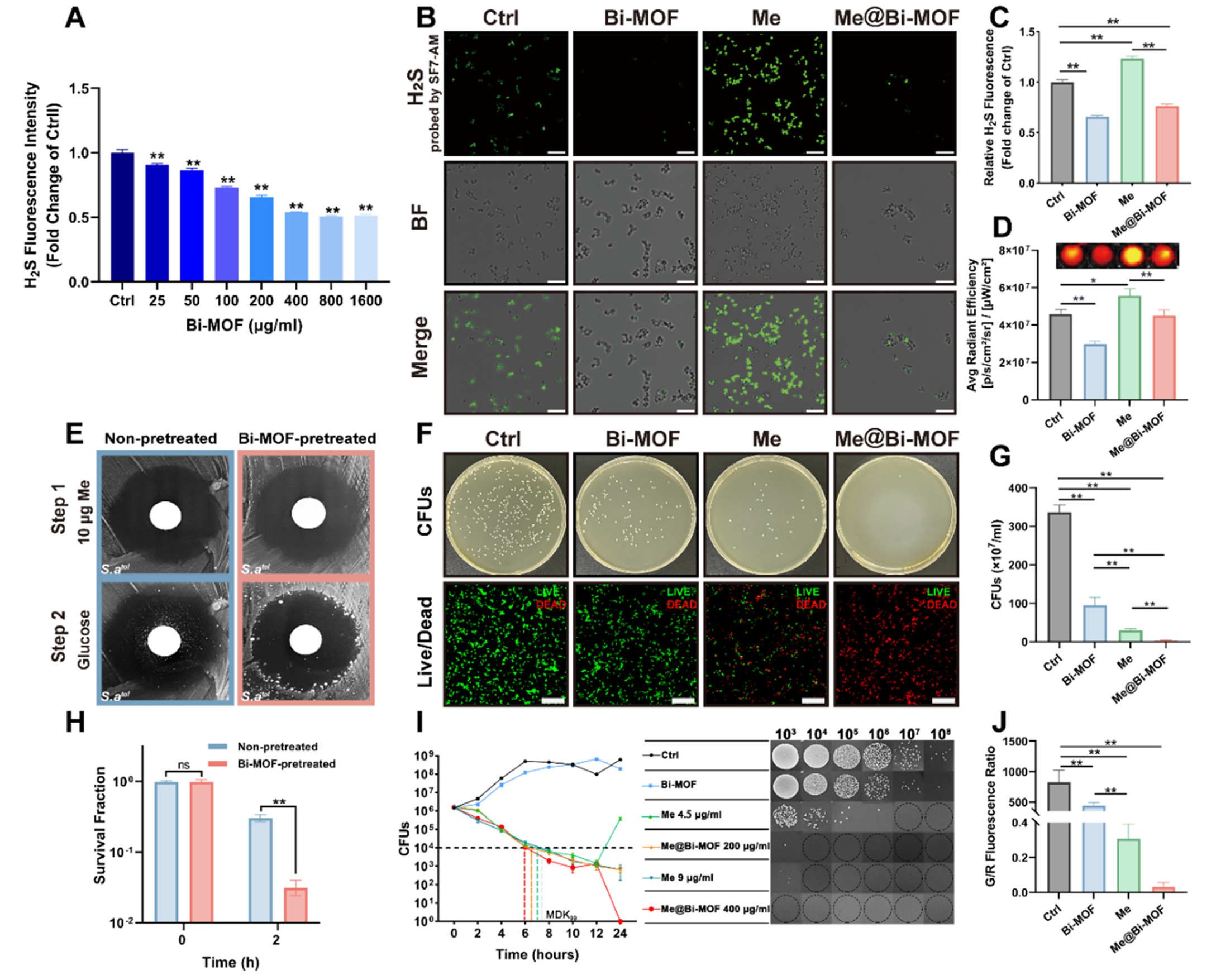
图3 Bi-MOF抑制细胞内H2S水平,协同增强甲氧西林对耐受菌的根除效果
4. 多组学分析揭示Bi-MOF作用的潜在机制
基于蛋白质组学和代谢组学的多组学分析,发现Bi-MOF处理导致细胞内发生强烈的蛋白毒性应激、能量动员和硫代谢,同时下调了与毒力因子和细胞壁合成相关的基因。这些潜在的机制,可能共同有助于增强甲氧西林对耐甲氧西林MRSA的杀菌效果(图4)。
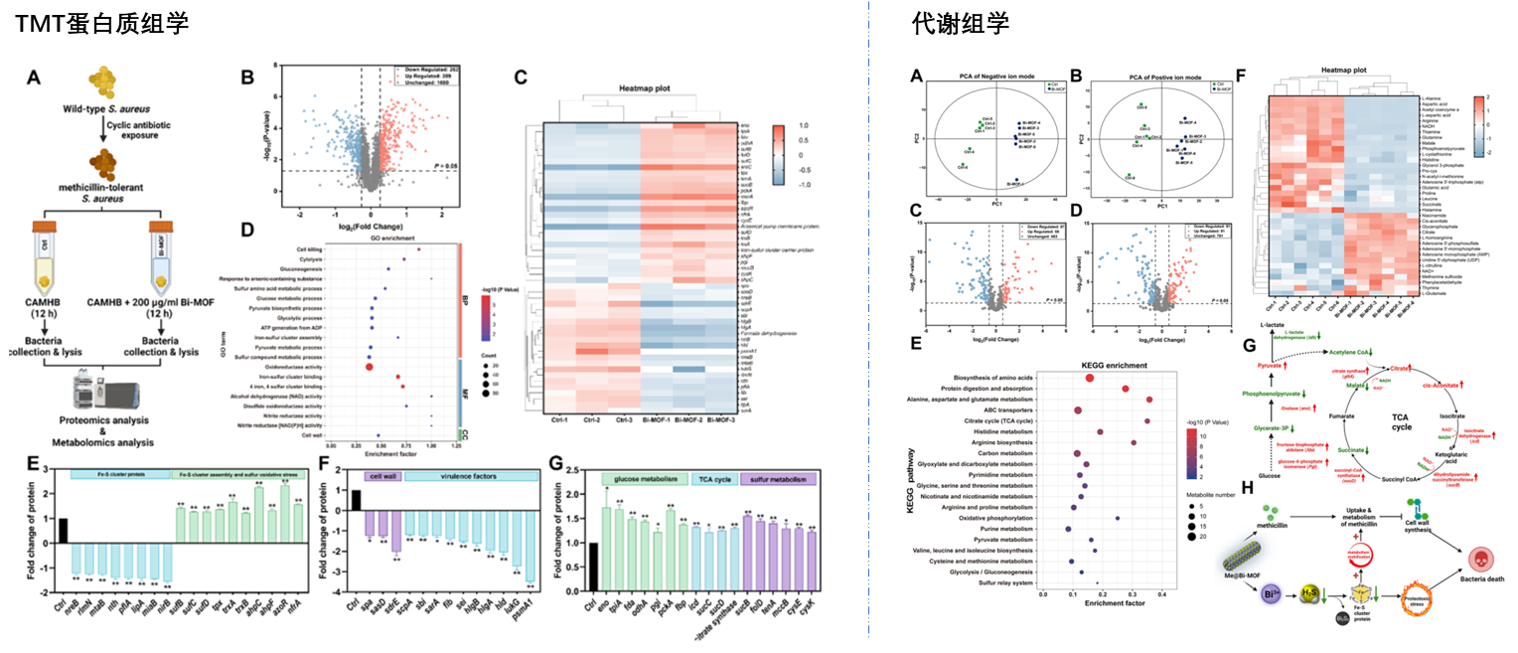
图4 Bi-MOF处理耐甲氧西林MRSA的多组学分析
5. Bi-MOF在体内感染早期检测中的应用
研究探索了Bi-MOF在活体小鼠皮下感染模型中的诊断性能。对小鼠进行PAI检测,结果显示Bi-MOF处理小鼠创面区域皮下腔内PAI信号强度呈时间依赖性升高,实时生成良好的对比图像(图5A-C)。该结果表明Bi-MOF与内源性细菌H2S反应生成Bi2S3,在激光刺激下产生满意的PAI信号。综上,Bi-MOF可作为一种具有空间信息的细菌感染实时精确检测工具。
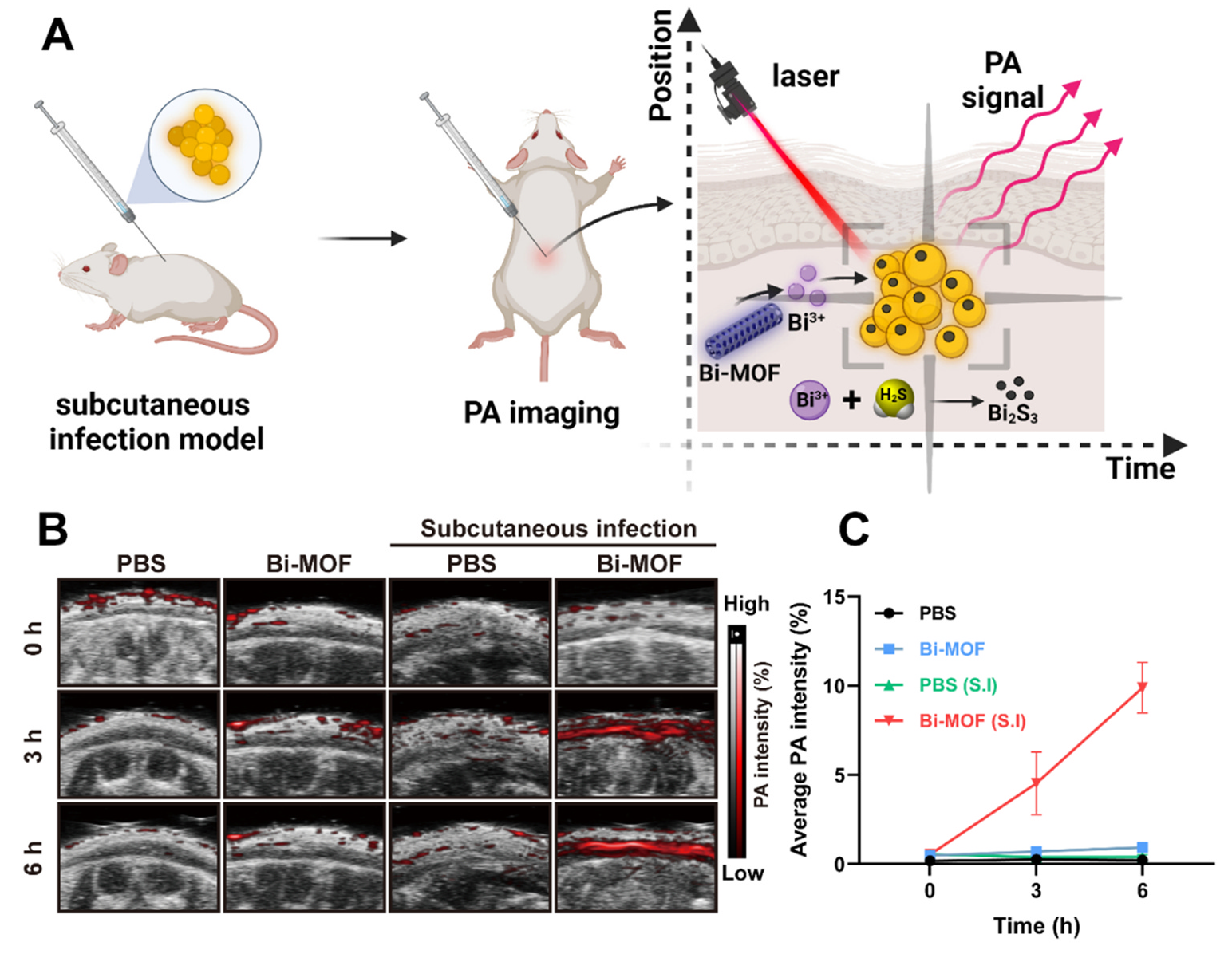
图5 Bi-MOF通过激光触发光声(PA)成像实现了感染的实时原位诊断
6. Bi-MOF在耐受型菌株诱导的小鼠皮下感染模型中可协同增强甲氧西林的治疗效果并抑制感染复发
通过建立耐甲氧西林MRSA皮下感染的小鼠模型,分别用甲氧西林单独或联合Bi-MOF进行5天的抗生素治疗,检测其体内治疗效果,其后再观察一周,检查感染是否再次发生。通过监测创面活菌载量、H2S水平等检测发现,甲氧西林的短期抗生素治疗促使耐受菌感染的短暂抑制,但不能完全根除,导致感染复发。Bi-MOF作为抗生素增强剂,与甲氧西林协同作用,有效根除创面内的耐受菌,促进创面愈合,缓解炎症浸润(图6)。
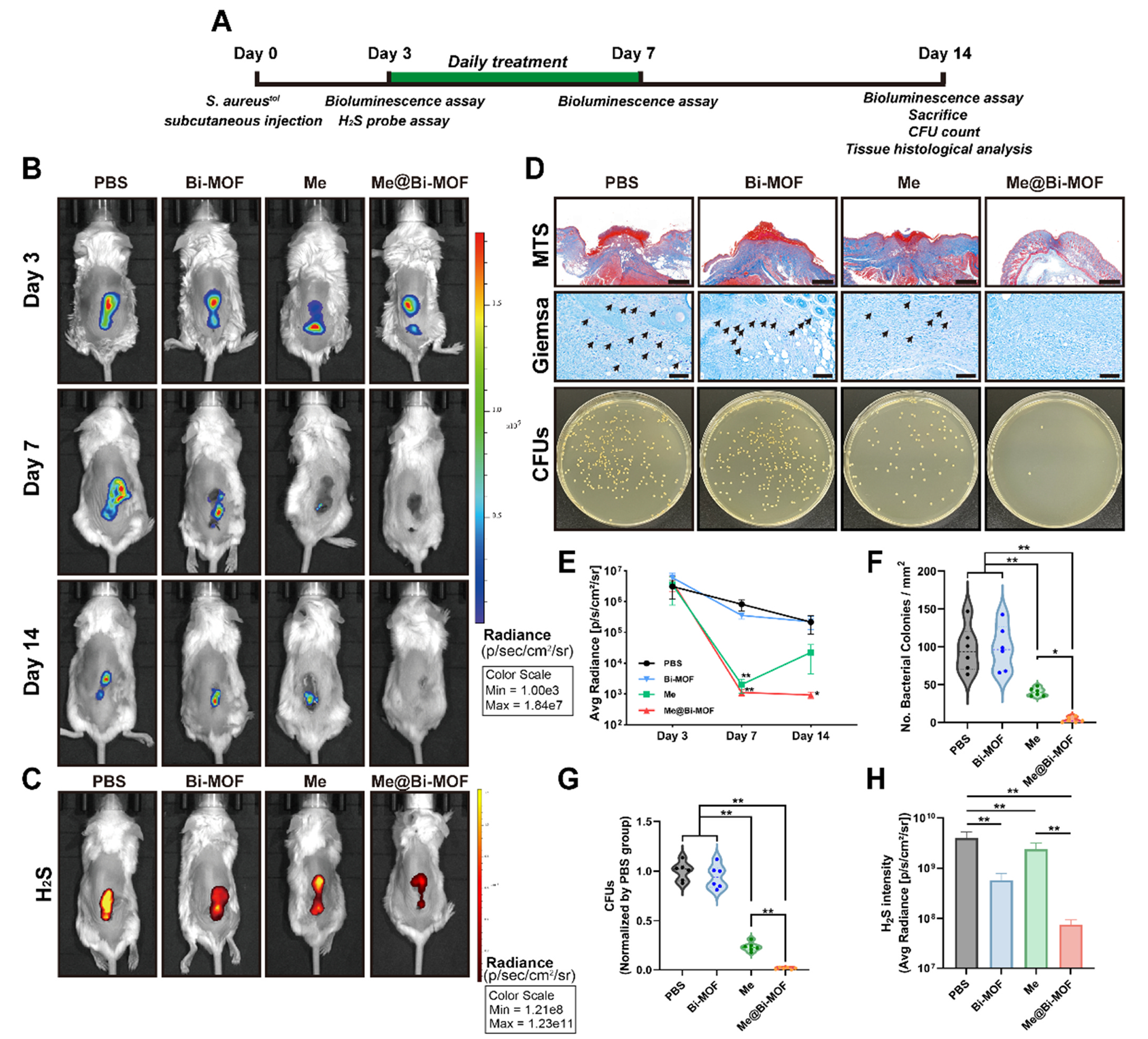
图6 Bi-MOF协同增强甲氧西林对耐甲氧西林MRSA的根除效果
小编小结
本研究合成了一种靶向耐受MRSA的治疗性抗生素增强剂,通过体内外实验证实,其可有效下调细菌细胞内H2S水平,根除耐甲氧西林MRSA感染,防止感染复发。此外,又通过多组学分析深入揭示了Bi-MOF治疗耐受菌的全景和其抗菌作用背后的详细机制。